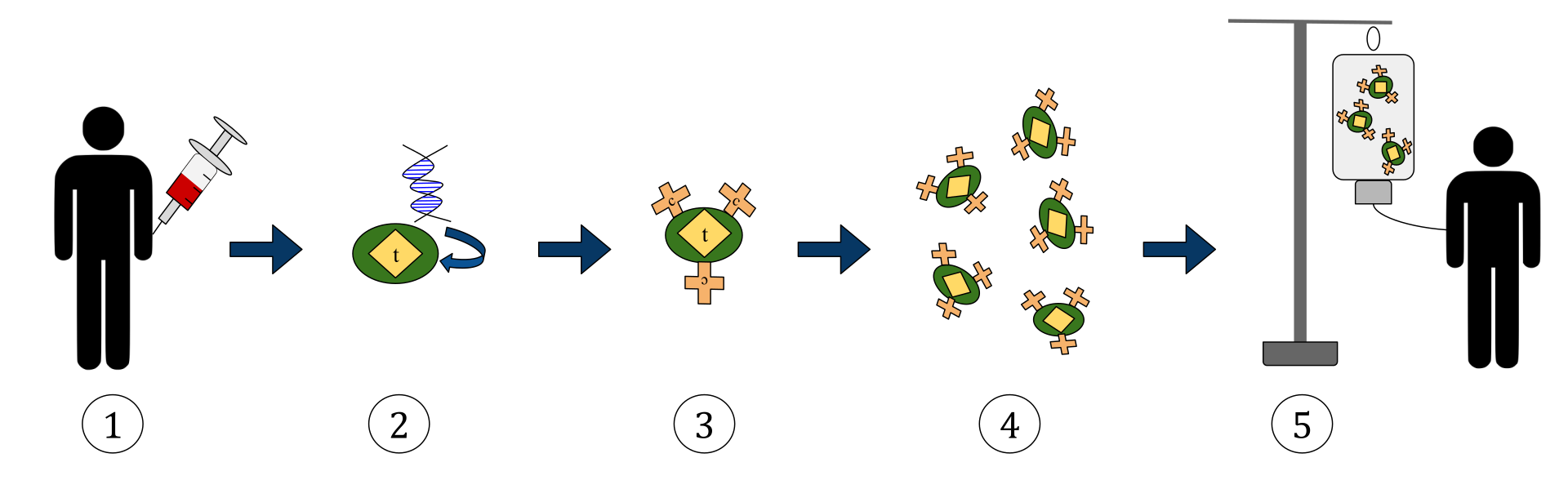
Rajah di atas mewakili proses terapi sel T reseptor antigen kimerik (CAR). Ini adalah kaedah imunoterapi, yang merupakan amalan yang semakin meningkat dalam rawatan barah. Hasil akhirnya ialah pengeluaran sel-T yang dilengkapi yang dapat mengenali dan melawan sel-sel barah yang dijangkiti di dalam badan.
1. Sel T (diwakili oleh objek yang dilabelkan sebagai ‘t’) dikeluarkan dari darah pesakit.
2. Kemudian di makmal menetapkan gen yang mengekod reseptor antigen tertentu dimasukkan ke dalam sel-T.
3. Oleh itu menghasilkan reseptor CAR (dilabelkan sebagai c) di permukaan sel.
4. Sel-sel T yang baru diubah suai kemudiannya dituai dan ditanam di makmal.
5. Setelah jangka waktu tertentu, sel T yang direkayasa dimasukkan kembali ke pesakit.
Sel T reseptor antigen chimeric (juga dikenali sebagai Sel-sel T KERETAadalah sel T yang telah direkayasa secara genetik untuk menghasilkan reseptor sel T buatan untuk digunakan dalam imunoterapi.
Reseptor antigen chimeric (KERETA, juga dikenali sebagai imunoreceptor chimeric, reseptor sel T chimeric, atau reseptor sel T tiruanadalah protein reseptor yang telah direkayasa untuk memberi sel T kemampuan baru untuk menargetkan protein tertentu. Reseptor bersifat kimerik kerana mereka menggabungkan fungsi pengikat antigen dan pengaktifan sel T menjadi reseptor tunggal.
Terapi sel CAR-T menggunakan sel T yang direkayasa dengan CAR untuk terapi barah. Premis imunoterapi CAR-T adalah untuk memodifikasi sel T untuk mengenali sel barah agar dapat mensasarkan dan memusnahkannya dengan lebih berkesan. Para saintis mengambil sel T dari orang, mengubahnya secara genetik, kemudian memasukkan sel CAR-T yang dihasilkan ke pesakit untuk menyerang tumor mereka. Sel-sel CAR-T boleh berasal dari sel-sel T dalam darah pesakit sendiri (autologous) atau berasal dari sel-sel T dari penderma lain yang sihat (allogeneic). Setelah diasingkan dari seseorang, sel T ini direkayasa secara genetik untuk mengekspresikan CAR tertentu, yang memprogramnya untuk menargetkan antigen yang ada di permukaan tumor. Untuk keselamatan, sel CAR-T direkayasa khusus untuk antigen yang dinyatakan pada tumor yang tidak dinyatakan pada sel yang sihat.
Setelah sel CAR-T dimasukkan ke dalam pasien, mereka bertindak sebagai “ubat hidup” terhadap sel barah. Ketika mereka bersentuhan dengan antigen yang disasarkan pada sel, sel CAR-T mengikatnya dan menjadi aktif, kemudian terus berkembang biak dan menjadi sitotoksik. Sel-sel CAR-T memusnahkan sel melalui beberapa mekanisme, termasuk percambahan sel yang banyak dirangsang, meningkatkan tahap toksiknya kepada sel-sel hidup lain (sitotoksisitas) dan dengan menyebabkan peningkatan rembesan faktor-faktor yang dapat mempengaruhi sel-sel lain seperti sitokin, interleukin dan faktor pertumbuhan.
Pengeluaran sel CAR-T

Langkah pertama dalam penghasilan sel CAR-T adalah pengasingan sel T dari darah manusia. Sel-sel CAR-T boleh dibuat sama ada dari darah pesakit itu sendiri, yang dikenali sebagai rawatan autologous, atau dari darah penderma yang sihat, yang dikenali sebagai rawatan allogenik. Proses pembuatannya sama dalam kedua-dua kes tersebut; hanya pilihan penderma darah awal yang berbeza.
Pertama, leukosit diasingkan menggunakan pemisah sel darah dalam proses yang dikenali sebagai apheresis leukosit. Sel mononuklear darah periferal (PBMC) kemudian dipisahkan dan dikumpulkan. Produk apheresis leukosit kemudian dipindahkan ke pusat pemprosesan sel. Di pusat pemprosesan sel, sel T tertentu dirangsang sehingga mereka akan aktif berkembang biak dan berkembang menjadi sebilangan besar. Untuk mendorong pengembangannya, sel T biasanya dirawat dengan antibodi sitokin interleukin 2 (IL-2) dan anti-CD3.
Sel T yang diperluas disucikan dan kemudian ditransduksi dengan gen yang menyandi CAR yang direkayasa melalui vektor retroviral, biasanya sama ada vektor gammaretrovirus (RV) atau vektor lentivirus (LV). Vektor ini sangat selamat pada zaman moden kerana penghapusan sebahagian wilayah U3. Alat penyuntingan gen baru CRISPR / Cas9 baru-baru ini digunakan sebagai ganti vektor retroviral untuk mengintegrasikan gen CAR ke laman web tertentu dalam genom.
Pesakit menjalani kemoterapi limfodepletion sebelum pengenalan sel CAR-T yang direkayasa. Penurunan jumlah leukosit yang beredar pada pesakit meningkatkan jumlah sitokin yang dihasilkan dan mengurangkan persaingan untuk mendapatkan sumber daya, yang membantu mendorong pengembangan sel CAR-T yang direkayasa.
Aplikasi klinikal
Sehingga Mac 2019, terdapat sekitar 364 ujian klinikal yang sedang berlangsung di seluruh dunia yang melibatkan sel-sel CAR-T. Sebilangan besar ujian tersebut mensasarkan kanser darah: terapi CAR-T menyumbang lebih daripada separuh daripada semua ujian untuk keganasan hematologi. CD19 terus menjadi sasaran antigen yang paling popular, diikuti oleh BCMA (biasanya dinyatakan dalam pelbagai myeloma). Pada tahun 2016, kajian mula meneroka daya maju antigen lain, seperti CD20. Ujian untuk tumor pepejal kurang dikuasai oleh CAR-T, dengan kira-kira separuh daripada percubaan berdasarkan terapi sel yang melibatkan platform lain seperti sel NK.
Kanser
Sel T direkayasa secara genetik untuk mengekspresikan reseptor antigen chimeric yang secara khusus ditujukan ke arah antigen pada sel tumor pesakit, kemudian dimasukkan ke dalam pesakit di mana mereka menyerang dan membunuh sel barah. Pemindahan sel T yang mengekspresikan CAR secara positif adalah terapi anti-kanser yang menjanjikan, kerana Sel T yang diubahsuai CAR dapat direkayasa untuk menargetkan hampir semua antigen yang berkaitan dengan tumor.
Penyelidikan sel CAR-T awal telah menumpukan pada kanser darah. Rawatan pertama yang diluluskan menggunakan CAR yang menargetkan antigen CD19, terdapat pada kanser yang berasal dari sel B seperti leukemia limfoblastik akut (SEMUA) dan limfoma sel B besar (DLBCL). Terdapat juga usaha yang sedang dijalankan untuk merekayasa CAR yang mensasarkan banyak antigen barah darah lain, termasuk CD30 pada limfoma Hodgkin refraktori; CD33, CD123, dan FLT3 dalam leukemia myeloid akut (AML); dan BCMA dalam pelbagai myeloma.
Tumor padat telah menunjukkan sasaran yang lebih sukar. Pengenalpastian antigen yang baik telah menantang: antigen semacam itu mesti dinyatakan pada kebanyakan sel barah, tetapi sebahagian besarnya tidak terdapat pada tisu normal. Sel CAR-T juga tidak diperdagangkan secara efisien ke pusat massa tumor pepejal, dan persekitaran mikro tumor yang bermusuhan menekan aktiviti sel T.
Penyakit autoimun
Walaupun kebanyakan kajian sel T CAR memfokuskan pada membuat sel T CAR yang dapat membasmi populasi sel tertentu (misalnya, sel T CAR yang menargetkan sel limfoma), ada potensi penggunaan lain untuk teknologi ini. Sel-T juga dapat melindungi antigen diri dari reaksi autoimun. Sel T sel pengatur yang dilengkapi dengan CAR dapat berpotensi memberikan toleransi terhadap antigen tertentu, sesuatu yang dapat digunakan dalam pemindahan organ atau penyakit reumatik seperti lupus.
Satefy
Terdapat kesan sampingan yang serius akibat sel CAR-T dimasukkan ke dalam badan, termasuk sindrom pelepasan sitokin dan ketoksikan neurologi. Oleh kerana ia adalah rawatan yang agak baru, ada sedikit data mengenai kesan jangka panjang terapi sel CAR-T. Masih ada kebimbangan mengenai kelangsungan hidup pesakit jangka panjang, serta komplikasi kehamilan pada pesakit wanita yang dirawat dengan sel CAR-T. Anafilaksis adalah kesan sampingan yang diharapkan, kerana CAR dibuat dengan antibodi monoklonal asing dan sebagai akibatnya, menimbulkan tindak balas imun.
Pengenalan pada sasaran / luar tumor berlaku apabila sel CAR-T mengenali antigen yang betul, tetapi antigen dinyatakan pada tisu yang tidak patogenik yang sihat. Ini mengakibatkan sel CAR-T menyerang tisu bukan tumor, seperti sel B yang sihat yang mengekspresikan CD19. Keterukan kesan buruk ini boleh berbeza-beza dari aplasia sel-B, yang dapat diatasi dengan infus sokongan, hingga toksisitas yang melampau yang menyebabkan kematian.
Terdapat juga kemungkinan yang tidak mungkin sel CAR-T yang direkayasa akan berubah menjadi sel barah melalui mutagenesis penyisipan, kerana vektor virus memasukkan gen CAR ke dalam penekan tumor atau onkogen dalam genom sel T inang. Beberapa vektor retroviral (RV) mempunyai risiko yang lebih rendah daripada vektor lentiviral (LV). Walau bagaimanapun, kedua-duanya berpotensi menjadi onkogenik. Analisis penjujukan genom dari laman penyisipan CAR di sel T telah dibuat untuk pemahaman yang lebih baik mengenai fungsi sel T CAR dan ketekunan dalam vivo.
Sindrom pelepasan sitokin
Masalah yang paling biasa selepas rawatan dengan sel CAR-T adalah sindrom pelepasan sitokin (CRS), suatu keadaan di mana sistem imun diaktifkan dan melepaskan peningkatan jumlah sitokin keradangan. Manifestasi klinikal sindrom ini menyerupai sepsis dengan demam tinggi, keletihan, mialgia, mual, kebocoran kapilari, takikardia dan disfungsi jantung lain, kegagalan hati, dan gangguan buah pinggang. CRS berlaku pada hampir semua pesakit yang dirawat dengan terapi sel CAR-T; sebenarnya, kehadiran CRS adalah penanda diagnostik yang menunjukkan sel CAR-T berfungsi sebagaimana dimaksudkan untuk membunuh sel barah. Namun, perhatikan bahawa tahap keparahan CRS yang lebih tinggi tidak berkorelasi dengan peningkatan tindak balas terhadap rawatan, tetapi beban penyakit yang lebih tinggi.
Neurotoksisiti berkaitan sel efektor
Ketoksikan neurologi juga sering dikaitkan dengan rawatan sel CAR-T. Mekanisme asasnya kurang difahami, dan mungkin atau mungkin tidak berkaitan dengan CRS. Manifestasi klinikal merangkumi kecelaruan, kehilangan sebahagian kemampuan untuk bercakap secara koheren sementara masih mempunyai kemampuan untuk menafsirkan bahasa (afasia ekspresif), kewaspadaan yang rendah (gangguan), dan kejang. Semasa beberapa ujian klinikal, kematian yang disebabkan oleh neurotoksisitas telah berlaku. Penyebab utama kematian akibat neurotoksisiti adalah edema serebrum. Dalam kajian yang dilakukan oleh Juno Therapeutics, Inc., lima pesakit yang mendaftar dalam percubaan itu mati akibat edema serebrum. Dua pesakit dirawat dengan siklofosfamid sahaja dan tiga yang lain dirawat dengan kombinasi siklofosfamid dan fludarabin. Dalam satu percubaan klinikal lain yang ditaja oleh Pusat Penyelidikan Kanser Fred Hutchinson, terdapat satu kes yang dilaporkan mengenai keracunan neurologi yang tidak dapat dipulihkan dan membawa maut 122 hari selepas pemberian sel CAR-T.
.
















